Actualité du Fares
La rifampicine désormais remboursée pour le traitement de l'infection tuberculose latente
Depuis le 1er mai 2024, la rifampicine est remboursée pour le traitement de l’infection tuberculose latente (ITL) aux mêmes conditions que la tuberculose active. Trois schémas, équivalents en termes d’efficacité, sont actuellement recommandés chez l’adulte et l’enfant : – Isoniazide (INH) 7jours/7 pendant 6 mois. – Rifampicine (RMP) 7jours/7 pendant 4 mois. – INH + RMP 7jours/7 pendant 3 mois. L’utilisation de la rifampicine permet de raccourcir la durée du traitement préventif et ainsi, d’améliorer la compliance du patient. Seul l’isoniazide était remboursé par l’INAMI pour le traitement de l’infection tuberculeuse. Désormais, comme stipulé dans la liste des spécialités (cf. chapitre IV, § 40200 : liste_specialites_chapter4part1_20240501.pdf (fgov.be) la rifampicine fait l’objet d’un remboursement en catégorie A, tant pour l’ITL que pour la tuberculose active. Comme pour le traitement de la tuberculose active, elle nécessite l’autorisation du médecin conseil. Pour introduire la demande de remboursement, connectez-vous sur CIVARS :
Pas au top : manque d'accès au traitement optimal de la TB-MDR et aux tests de résistance en Europe
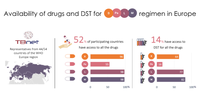
La tuberculose est l'une des principales maladies infectieuses responsables de décès dans le monde. La tuberculose multirésistante (TB-MDR) (ou résistante à la rifampicine (TB-RR)), est particulièrement difficile à traiter et représente une menace sérieuse dans la lutte contre cette maladie, au niveau international. En mai 2022, l'Organisation mondiale de la santé (OMS) a recommandé un nouveau régime de traitement plus court (6 mois) et entièrement oral comme étant la meilleure option pour traiter les patients atteints de TB-MDR/TB-RR. Ce nouveau traitement, connu sous l’acronyme BPaLM, comprend quatre médicaments : la bedaquiline, la pretomanide, la linezolide et la moxifloxacine. Le BPaLM s’avère être très efficace et, surtout, avoir moins d'effets indésirables, par rapport aux régimes prescrits antérieurement. En effet, jusqu'à il y a peu, la TB-MDR/TB-RR nécessitait 18 mois de traitement et souvent avec des injections douloureuses quotidiennes pendant les premiers mois. Un grand nombre de patients recevant ces traitements de 18 mois souffrait d'effets secondaires graves, qui pouvaient conduire à l’arrêt prématuré du traitement et la non-guérison. Compte tenu de tout cela, l'approbation de ce nouveau schéma thérapeutique peut être définie comme un "changement de paradigme" dans le traitement de la TB-MDR/TB-RR. Cependant, cette avancée majeure est en péril. Les rapports montrent l’augmentation de la résistance antimicrobienne à ces nouveaux médicaments contre la TB. Des données précoces suggèrent que la bedaquiline, l'un des principaux médicaments de ce nouveau régime TB-MDR/TB-RR, pourrait être particulièrement sujette au développement de la résistance. Pour prévenir le développement de nouvelles résistances, il est nécessaire de fournir un traitement avec des médicaments efficaces à chaque patient et pour cela, des tests de résistance doivent être effectués en temps opportun. Durant l'automne 2023, TBnet (Tuberculosis Network European Trials group) a posé la question pour savoir si, un an après la publication des nouvelles recommandations par l’OMS, les patients en Europe ont accès ou non au nouveau régime de traitement et aux tests de résistance pour ces nouveaux médicaments. Des 54 pays de la région européenne de l'OMS, 44 pays dont la Belgique, ont répondu à l'enquête et les résultats sont interpelant : seuls 52% des pays ont accès aux 4 médicaments du schéma BPaLM, l’indisponibilité la plus fréquente étant celle de la pretomanide (55%). Pire encore, seulement14% des pays déclarent avoir accès aux tests de résistance aux quatre médicaments du nouveau régime de traitement, l'accès étant limité essentiellement à la bedaquiline (64%) et à la pretomanide (16%). Ces résultats complètent ceux d'une enquête antérieure de TBnet qui avait montré des coûts disproportionnés dans la prise en charge de la TB-MDR/TB-RR dans les pays européens, où par ailleurs, le manque d'accès aux médicaments ne se limitait pas seulement aux médicaments TB-MDR/TB-RR, mais également aux médicaments nécessaires à la prise en charge des tuberculoses sensibles et des infections tuberculeuses latentes dans la région européenne de l'OMS. De même, une enquête récente du ptbnet, un réseau européen de la tuberculose pédiatrique, a documenté d'importants défis pour accéder aux formulations pédiatriques pour traiter la tuberculose en Europe. Dr. G. Günther, l'un des auteurs de la publication des résultats de l'enquête de 2023 dans le journal "Clinical Microbiology and Infection", déclare : "Les patients atteints de TB-MDR/TB-RR ont le droit d'avoir accès au meilleur schéma thérapeutique : actuellement, ce n'est le cas que pour un peu plus de la moitié des patients en Europe. En parallèle, nous devons rapidement augmenter l'accès aux tests de résistance à ces nouveaux médicaments. Sinon, nous pourrions rapidement perdre notre meilleure et plus efficace innovation en matière de soins de la tuberculose depuis des décennies à cause de la résistance émergente. Les soins de la tuberculose en Europe sont compromis par le manque d'accès aux médicaments salvateurs et au diagnostic optimal, et cela est inacceptable." Référence: Other publications from TBnet on access to MDR-TB drugs and drug resistance testing in Europe:
Availability of drugs and resistance testing for BPaLM regimen for rifampicin-resistant tuberculosis in Europe.
Clinical Microbiology and Infection. 2024 Mar 13 [cited 2024 Mar 14];0(0). Available from: https://www.clinicalmicrobiologyandinfection.com/article/S1198-743X(24)00121-6/abstract
Availability and costs of medicines for the treatment of tuberculosis in Europe.
Clinical Microbiology and Infection. 2023 Jan;29(1):77-84. doi: 10.1016/j.cmi.2022.07.026.
European Respiratory Journal. 2022 May 19;59(5):2200388.
Relative cost of multidrug-resistant TB medicines in Europe.
International Journal of Tuberculosis and Lung Diseases. 2023 May 1;27(5):341-344.
Availability of fixed-dose, child-friendly formulations of first-line tuberculosis drugs in Europe.
European Respiratory Journal 2021; Oct 1;58(3):2101196.
Arrêt de commercialisation de la Pyridoxine LABAZ
Selon l’AFPMS, la Pyridoxine LABAZ n’est plus commercialisée en Belgique. Ce médicament est nécessaire pour contrer certains effets secondaires du traitement de la tuberculose. Pour pallier à cette rupture, la solution est de le remplacer par le Befact Forte qui comprend de la Pyridoxine LABAZ (vit B6) 250mg mais également d’autres vitamines (B1, B2 et B12). Le coût est d’environ 10€ non remboursé par la mutuelle contre 4€ pour la pyridoxine LABAZ, donc un surcoût d’environ 6€. Si votre patient éprouve des difficultés financières à payer ce médicament, vous pouvez demander une prise en charge à BELTA-TBnet.







